Los electrodos de puesta a tierra fabricados con un material uniforme pueden verse amenazados por la corrosión proveniente de los suelos corrosivos y la formación de celdas de concentración. El riesgo de corrosión de los suelos corrosivos depende del material y del tipo y de la composición del suelo.
La aislación eléctrica de las instalaciones que actúan como ánodos para evitar la formación de estas celdas solo es posible en casos excepcionales. Hoy en día, el objetivo es integrar todos los electrodos de puesta a tierra, incluidas las instalaciones de metal conectadas a tierra para poder lograr la conexión equipotencial y, en consecuencia, la máxima seguridad contra tensiones con riesgo de choque por fallas o impactos de rayos.
En las instalaciones de alta tensión, los electrodos de puesta a tierra de protección contra alta tensión cada vez más se conectan a electrodos de puesta a tierra que operan a baja tensión, conforme la norma HD 63751. Asimismo, las normas IEC 60364-4-41 (2005) y HD 60364-41(2007) requieren de la integración de conductos y demás instalaciones en las medidas de protección contra riesgo de choque eléctrico. Así, la única manera de prevenir o, por lo menos, reducir el riesgo de corrosión de los electrodos de puesta a tierra y demás instalaciones en contacto con ellos es elegir materiales adecuados para la fabricación de electrodos de puesta a tierra.
La norma DIN VDE 0151 titulada “Material y dimensiones mínimas de electrodos de puesta a tierra respecto de la corrosión” está a disposición desde junio de 1986 como documento oficial. Además de décadas de experiencia en el campo de la tecnología de puesta a tierra, esta norma incluye, también, los resultados de exámenes preliminares extensivos. Están disponibles muchos resultados interesantes que son importantes para los electrodos de puesta a tierra, incluidos los de los sistemas de protección contra rayos.
A continuación, se explican los procesos fundamentales que llevan a la corrosión. De los conocimientos adquiridos por el grupo de trabajo VDE “materiales de la puesta tierra” se derivan las medidas prácticas anticorrosivas y de conservación del buen estado del material, especialmente en lo que respecta a los electrodos de puesta tierra para la protección contra las descargas atmosféricas.
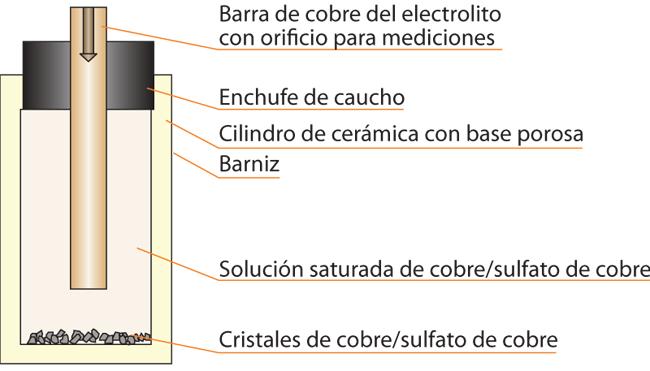 Figura 1. Ejemplo de aplicación de un electrodo de medición no polarizable (electrodo de cobre/sulfato de cobre) para adquirir un potencial dentro del electrolito (vista de sección transversal)
Figura 1. Ejemplo de aplicación de un electrodo de medición no polarizable (electrodo de cobre/sulfato de cobre) para adquirir un potencial dentro del electrolito (vista de sección transversal)- Corrosión. Reacción de un material de metal con el entorno, que lleva al deterioro de las características de dicho material y/o de su entorno. Por lo general, la reacción es de carácter electroquímico.
- Corrosión electroquímica. Corrosión durante la cual tienen lugar los procesos electroquímicos. Se producen exclusivamente en presencia de un electrolito.
- Electrolito. Medio corrosivo conductor de iones (por ejemplo, suelo, agua, sales fundidas).
- Electrodo. Material conductor de electrones en un electrolito. El sistema de electrodo y electrolito forma una media celda.
- Ánodo. Electrodo desde el cual una corriente continua ingresa al electrolito.
- Cátodo. Electrodo desde el cual una corriente continua deja el electrolito.
- Electrodo de referencia. Electrodo de medición para determinar el potencial de un metal en el electrolito.
- Electrodo de cobre/sulfato de cobre. Electrodo de referencia que apenas puede polarizarse, fabricado de cobre en una solución saturada de sulfato de cobre. El electrodo de sulfato de cobre es la forma más común del electrodo de referencia para la medición del potencial de objetos metálicos subterráneos (figura 1).
- Celda de corrosión. Celda voltaica con diferentes densidades locales de corrientes parciales para disolver el metal. Pueden formarse ánodos y cátodos de la celda de corrosión a) en el material, por diferentes metales (corrosión por contacto) o por diferentes componentes estructurales (corrosión selectiva o intercristalina); b) en el electrolito, por diferentes concentraciones de determinados materiales con características estimulantes o inhibitorias para disolver el metal.
- Potenciales. a) Potencial de referencia. Potencial de un electrodo de referencia respecto del electrodo de hidrógeno estándar; b) Potencial eléctrico de un metal. Potencial eléctrico de un metal o de un sólido conductor de electrones en un electrolito.
Dependiendo de la magnitud de ambas presiones, o bien, los iones de metal de la varilla pasan a la solución (por lo que la varilla se convierte en negativa respecto de la solución) o los iones del electrolito se agrupan en grandes números en la varilla (la varilla se torna positiva respecto del electrolito). Así, se crea una tensión entre dos varillas de metal en el electrolito.
Considérese el caso de dos varillas fabricadas con diferentes metales que se sumergen en el mismo electrolito: se crea ahora una tensión de determinada magnitud en cada varilla del electrolito. Puede utilizarse un voltímetro para medir la tensión entre varillas (electrodos), esta es la diferencia entre los potenciales de los electrodos individuales respecto del electrolito. ¿De qué manera surge ahora que la corriente fluye en el electrolito y, por lo tanto, que el material se transporta, es decir, se produce la corrosión?
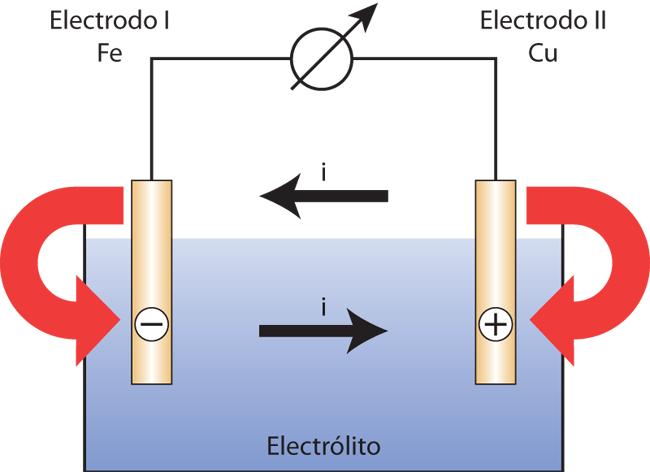
Si, según se muestra en este documento, los electrodos de cobre y hierro se conectan mediante un amperímetro fuera del electrolito, por ejemplo, se verifica lo que muestra la figura 2, en el circuito exterior, la corriente i fluye de positivo (+) a negativo (-), es decir, del electrodo de cobre “más noble" de acuerdo con la tabla 1, al electrodo de hierro.
Por otro lado, en el electrolito, la corriente i debe fluir del electrodo de hierro “más negativo” al electrodo de cobre para cerrar el circuito. A modo de generalización, ello significa que del polo más negativo pasan los iones positivos al electrolito y, por lo tanto, se convierte en el ánodo de la celda voltaica, es decir, se disuelve.
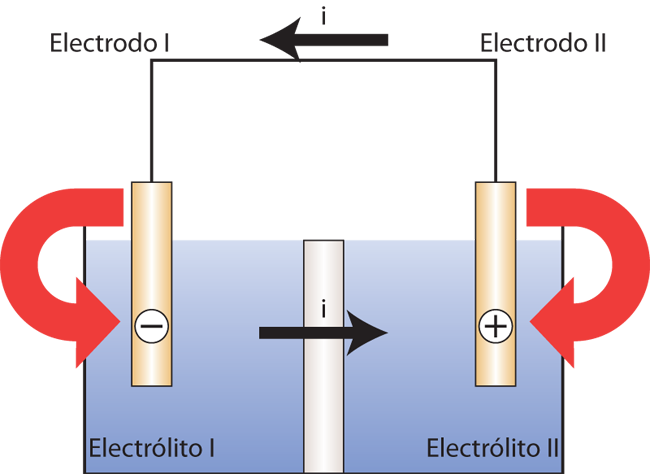
La disolución del metal tiene lugar en estos puntos, donde la corriente ingresa al electrolito. También puede surgir una corriente de corrosión a partir de una celda de concentración (figura 3). En este caso, dos electrodos del mismo tipo de metal se sumergen en diferentes electrolitos. El electrodo en el electrolito II que tiene la mayor concentración de iones de metal se torna eléctricamente más positivo que el otro. La conexión de ambos electrodos permite que la corriente i fluya y el electrodo, que es más negativo desde el punto de vista electroquímico, se disuelva.
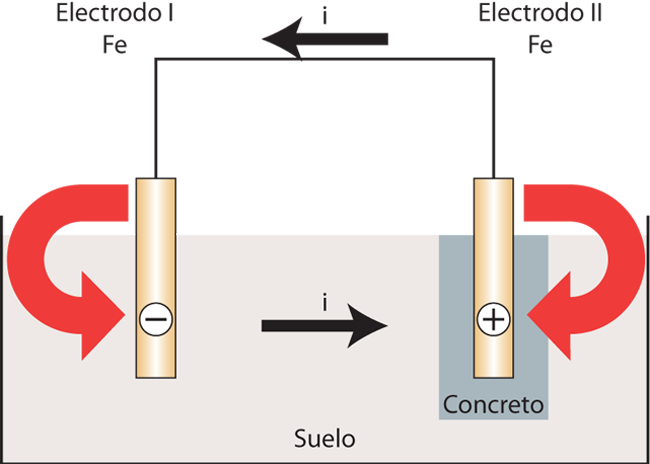
Puede formarse una celda de concentración de este tipo, por ejemplo, por dos electrodos de hierro, uno de los cuales se fija en el hormigón; mientras el otro queda en tierra (figura 4).
| Definición | Cobre | Plomo | Latón | Hierro | Zinc |
|---|---|---|---|---|---|
| Potencial de corrosión libre en el suelo (UM-Cu/CuSO4) (1) | 0 a 0,1 V | -0,5 a -0,6 V | -0,4 a -0,6 V (2) | -0,5 a -0,8 V (3) | -0,9 a -1,1 V (5) |
| Potencial de protección catódica en el suelo (UM-Cu/CuSO4) (1) | -0,2 V | -0,65 V | -0,65 V (2) | -0,85 V (4) | -1,2 V (5) |
| Equivalente electroquímico (K = [Δm/lt]) | 10,4 kg/año | 33,9 kg/año | 19,4 kg/año | 9,1 kg/año | 10,7 kg/año |
| Velocidad de corrosión lineal a J = 1 mA/dm² (W = [Δs/t]) | 0,12 mm/año | 0,3 mm/año | 0,27 mm/año | 0,12 mm/año | 0,15 mm/año |
Tabla 1. Valores potenciales y tasas de corrosión de materiales de metal común
(1) Medida con el electrodo de cobre/sulfato de cobre saturado (Cu/CuSO4) | (2) Valores verificados en ensayos realizados. El potencial del cobre revestido en latón depende del espesor del recubrimiento de latón. Los recubrimientos de latón comunes hasta el presente representan una pocos micrones y, por lo tanto, se encuentran entre los valores del latón y el cobre en el suelo. | (3)Estos valores también se aplican a tipos de hierro de menor aleación. El potencial del acero en el hormigón (armaduras de fundaciones) depende considerablemente de influencias externas. Medido con un electrodo saturado de cobre/sulfato de cobre, generalmente representa de -0,1 a 0,4 volts. En el caso de conexiones conductoras de metal con amplias instalaciones subterráneas de metal con potencial más negativo, se polariza catódicamente y, por lo tanto, alcanza valores de hasta aproximadamente 0,5 volts. | (4) En suelos anaeróbicos, el potencial de protección debería ser de -0,95 volts. | (5) Acero galvanizado por inmersión en caliente, con recubrimiento de zinc, que posee una capa de zinc pura externa y cerrada. El potencial del acero galvanizado por inmersión en caliente en el suelo, por lo tanto, corresponde a aproximadamente el valor indicado de zinc en el suelo. En caso de pérdida de la capa de zinc, el potencial se hace más positivo. Con esta corrosión completa, puede alcanzar el valor del acero. El potencial del acero galvanizado por inmersión en caliente en el hormigón posee aproximadamente los mismos valores iniciales. Con el tiempo, el potencial se hace más positivo. Sin embargo, todavía no se hallaron valores más positivos de aproximadamente -0,75 volts. El cobre enérgicamente galvanizado por inmersión en caliente con una capa de zinc de, por lo menos, setenta micrones también posee una capa externa cerrada de zinc puro. El potencial del cobre galvanizado por inmersión en caliente del suelo, por lo tanto, corresponde a aproximadamente el valor indicado de zinc en el suelo. En el caso de una capa de zinc más delgada o de corrosión de la capa de zinc, el potencial se hace más positivo. Aún no se han definido los valores límite.
Al conectar estos electrodos, el hierro en el hormigón se convierte en el cátodo de la celda de concentración y el que se queda en tierra se convierte en el ánodo; por lo tanto, este último se destruye por pérdida de iones.
Para la corrosión electroquímica, el caso generalmente es que, cuanto más grandes son los iones y menor es su carga, mayor es el transporte de metal asociado al flujo de corriente i (es decir, i es proporcional a la masa atómica del metal).
Sin embargo, de más interés práctico es la predicción de si, y durante cuánto período de tiempo, la corrosión causará orificios o picaduras por corrosión en los electrodos de puesta a tierra, tanques de acero, caños, etc. Por lo tanto, resulta importante si el ataque de la corriente presunta tendrá lugar de manera difusa o puntiforme.
Para el ataque corrosivo, no es solo la magnitud de la corriente de corrosión la que resulta decisiva; sino también y en especial, su densidad, es decir la corriente por unidad del área de descarga.
A menudo no se puede determinar directamente esta densidad de corriente. En esos casos, se maneja con mediciones de potencial desde los cuales puede tomarse el grado de polarización disponible. El comportamiento de los electrodos respecto de la polarización solo se debate superficialmente en este documento.
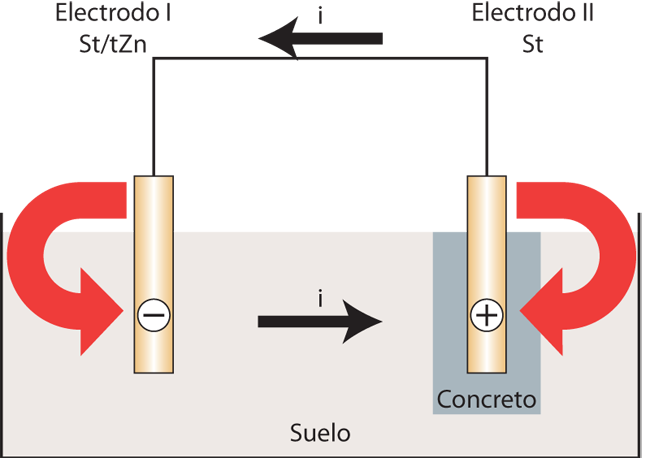
Considérese el caso de un fleje de acero galvanizado situado en tierra y conectado a la armadura de acero (negro) de una fundación de hormigón (figura 5). De acuerdo con nuestras mediciones, se producen aquí las siguientes diferencias de potencial respecto del electrodo de sulfato de cobre:
- Acero (desnudo) en hormigón: -200 milivolts
- Acero galvanizado en arena: -800 milivolts
Por lo general, se observa que la corriente i en tierra es generada por cambios en el material. Sin embargo, un cambio en el material también significa que la tensión de los metales individuales cambia respecto del suelo. Esta variación de potencial causada por la corriente de corrosión i se denomina polarización. La resistencia de la polarización es directamente proporcional a la densidad de la corriente. Ahora, los fenómenos de polarización tienen lugar en los electrodos negativos y positivos. Sin embargo, las densidades de corriente en ambos electrodos son muy diferentes.
A modo de ilustración, consideraremos el siguiente ejemplo: se conecta un caño de gas, de acero, con una buena aislación en tierra a electrodos de cobre de puesta a tierra. Si el caño con aislación solo posee unos pequeños puntos donde falta material, existe una mayor densidad de corriente en estos puntos como resultado de la corrosión rápida del acero. En oposición, la densidad de corriente es baja en el área más grande de los electrodos de puesta a tierra de cobre donde ingresa la corriente. Así, la polarización es mayor en el conductor de acero aislado más negativo que en los electrodos de puesta a tierra de cobre positivos. El potencial del conductor de acero cambia a valores más positivos. Así, también disminuye la diferencia de potencial entre los electrodos. Por lo tanto, la magnitud de la corriente de corrosión es también una función de las características de polarización de los electrodos.
La resistencia de polarización puede estimarse midiendo los potenciales de los electrodos de un circuito dividido. El circuito se divide para evitar la caída de tensión en el electrolito. Por lo general, para dichas mediciones se utilizan instrumentos de registro, pues frecuentemente existe una rápida despolarización inmediatamente después de interrumpida la corriente de corrosión.
Si ahora se mide la fuerte polarización en el ánodo (el electrodo más negativo), es decir, si hay un cambio obvio a potenciales más positivos, habrá un alto riesgo de corrosión del ánodo.
Volvamos a nuestra celda de corrosión–acero (desnudo) en hormigón/acero, galvanizado en la arena (figura 5). Respecto de un electrodo de sulfato de cobre distante, es posible medir un potencial de celdas interconectadas de entre -200 y -800 milivolts. El valor exacto depende de la relación del área anódica a catódica y de la polarizabilidad de los electrodos. Si, por ejemplo, el área de la fundación de hormigón armado es muy grande en comparación con la superficie del conductor de acero galvanizado, se producirá en el último una densidad de corriente anódica alta, que se polariza a prácticamente el potencial de la armadura de acero y se destruye en un período de tiempo relativamente corto. Así, la polarización positiva alta siempre indica un mayor riesgo de corrosión.
En la práctica, obviamente es ahora importante conocer el límite sobre el cual un cambio de potencial positivo significa un riesgo agudo de corrosión. Lamentablemente, no es posible indicar un valor definitivo que se aplique en cada caso; los efectos de las condiciones del suelo solamente son demasiado diversas. Sin embargo, es posible estipular campos de cambios de potencial para suelos naturales.
Resumiendo, se puede estipular que la condición previa para la formación de celdas de corrosión (celdas voltaicas) es siempre la presencia de ánodos y cátodos de metal conectados y electrolíticos que cierran el circuito conductivo.
Los ánodos y cátodos se forman a partir de a) materiales: diferentes metales o diferentes condiciones de superficies de un metal (corrosión por contacto), diferentes componentes estructurales (corrosión selectiva o intercristalina); b) electrolitos: diferente concentración (por ejemplo, salinidad, ventilación).
En las celdas de corrosión, los campos anódicos siempre poseen un potencial de metal/electrolito más negativo que los campos catódicos.
Los potenciales de metal/electrolito se miden utilizando un electrodo de cobre/sulfato de cobre saturado montado en los alrededores inmediatos del metal en el suelo o sobre este. Si existe una conexión conductora de metal entre el ánodo y el cátodo, la diferencia de potencial produce una corriente de continua en el electrolito que pasa desde el ánodo y se introduce en el electrolito disolviendo el metal antes de reingresar al cátodo.
Con frecuencia se aplica la regla de superficie para estimar la densidad de corriente anódica promedio IA:
- UA UC. Potenciales del ánodo o cátodo en volts
- φK. Resistencia de polarización específica del cátodo en Ωm2
- AA AC. Superficies del ánodo o cátodo en metros cuadrados
| Material de superficie pequeña | Acero galvanizado | Acero | Acero en hormigón | Cobre o acero inoxidable |
|---|---|---|---|---|
| Acero galvanizado | + | + | - | - |
| Acero | + | + | + | + |
| Acero en hormigón | + | + | + | + |
| Acero con revestimiento de cobre | + | + | + | + |
| Cobre/acero inoxidable | + | + | + | + |
Tabla 2. Combinaciones de materiales de sistemas de puesta a tierra para diferentes relaciones de superficie
La resistencia de polarización es la relación de la tensión de polarización y la corriente total de un electrodo mixto (un electrodo donde tiene lugar más de una reacción de electrodo).
En la práctica, es posible determinar las tensiones de excitación de celda UA - UC y el tamaño de las superficies AC y AA como una aproximación para estimar la tasa de corrosión. Sin embargo, los valores de φA (resistencia de polarización específica del ánodo) y φC no están disponibles en grado suficiente de precisión, sino que dependen de los materiales de los electrodos, los electrolitos y las densidades de corriente anódica y catódica.
Los resultados de los exámenes disponibles hasta ahora permiten concluir que φA es mucho más pequeño que φC.
Para φC se aplica lo siguiente:
- Acero en tierra: 1 Ωm2, aproximadamente
- Cobre en tierra: 5 Ωm2, aproximadamente
- Acero en hormigón: 30 Ωm2, aproximadamente
Al seleccionar materiales adecuados, es posible evitar o reducir el riesgo de corrosión de los electrodos de puesta a tierra. Para lograr una vida útil satisfactoria, se deben mantener las dimensiones mínimas del material (tabla 3).
| Material | Configuración | Barra de tierra | Conductor de tierra | Placa de tierra | Observaciones |
|---|---|---|---|---|---|
| Cobre | Cableado (3) | - | 50 mm² | - | Diámetro mínimo, 1,7 mm |
| Cobre | Barra maciza redonda (3) | - | 50 mm² | - | Diámetro 8 mm |
| Cobre | Placa maciza (3) | - | 50 mm² | - | Espesor 2 mm |
| Cobre | Barra maciza redonda | 15 mm (8) | - | - | - |
| Cobre | Cañería | 20 mm | - | - | Espesor mínimo de pared, 2 mm |
| Cobre | Placa maciza | - | - | 500 x 500 mm | Espesor mínimo, 2 mm |
| Cobre | Placa tipo rejilla | - | - | 600 x 600 mm | Longitud mínima, 4,8 mm |
| Acero | Barra redonda maciza galvanizada (1, 2) | 16 mm (9) | 10 mm | - | - |
| Acero | Cañería galvanizada (1, 2) | 25 mm | - | - | Espesor mínimo de pared, 2 mm |
| Acero | Planchuela galvanizada (1) | - | 90 mm² | - | Espesor mínimo, 3 mm |
| Acero | Placa maciza galvanizada (1) | - | - | 500 x 500 mm | Espesor mínimo, 3 mm |
| Acero | Placa tipo rejilla galvanizada (1) | - | - | 600 x 600 mm | 30 x 3 mm de sección |
| Acero | Barra redonda revestida de cobre (4) | 14 mm | - | - | Revestimiento de cobre, 250 μm |
| Acero | Barra redonda desnuda (5) | - | 10 mm | - | - |
| Acero | Placa maciza desnuda o galvanizada (5, 6) | - | 75 mm² | - | Espesor mínimo, 3 mm |
| Acero | Cableado galvanizado (5, 6) | - | 70 mm² | - | Diámetro mínimo de un alambre, 1,7 mm |
| Acero inoxidable (7) | Barra maciza redonda | 15 mm | 10 mm | - | - |
| Acero inoxidable (7) | Placa maciza | - | 100 mm² | - | Espesor mínimo, 2 mm |
Tabla 3. Material, configuración dimensiones mínimas de los electrodos de puesta a tierra, de acuerdo a la tabla 7 de la norma 62305-3
1) Los revestimientos deben ser lisos, continuos y libres de fundentes y manchas residuales, con un espesor | mínimo de cincuenta micrones para las barras redondas y setenta para las placas. | 2) Los materiales deben ser maquinados antes del galvanizado. | 3) Puede ser también revestido en estaño. | 4) Es conveniente que el cobre sea unido al acero de forma íntima. | 5) Admitido solamente si se incluyen completamente en el hormigón. | 6) Admitido solamente para la parte de la fundación en contacto con la tierra, si se conecta correctamente por lo menos cada cinco metros con las armaduras naturales de acero de la fundación. | 7) Cromo mayor o igual a disciséis por ciento, níquel mayor o igual a cinco por ciento, molibdeno mayor o igual a dos por ciento, carbono menor o igual a 0,08 por ciento. | 8) En algunos países, son admisibles valores de doce milímetros. | 9) En algunos países, se utiliza el electrodo de tierra para conectar el conductor de bajada en el punto de ingreso a tierra.
- Acero galvanizado por inmersión en caliente. El acero galvanizado por inmersión en caliente también es adecuado para empotrar en el hormigón. Los electrodos de puesta a tierra de fundación, los electrodos de puesta a tierra y los conductores con conexión equipotencial de acero galvanizado en el hormigón pueden estar conectados con las armaduras.
- Acero con vaina de cobre. En el caso del acero con vaina de cobre, los comentarios del cobre desnudo se aplican al material de la vaina. Sin embargo, el daño a la vaina de cobre genera un alto riesgo de corrosión del núcleo de acero; de ahí que siempre deba existir una capa de cobre cerrada completa.
- Cobre desnudo. El cobre desnudo es muy resistente debido a su posición en la calificación de aislación electrolítica. Asimismo, en combinación con los electrodos de puesta a tierra u otras instalaciones en tierra hechas de materiales más ‘básicos’ (por ejemplo, el acero), posee una protección catódica adicional, a pesar de ser a costa de los metales más básicos.
- Aceros inoxidables. Determinados aceros inoxidables altamente aleados de acuerdo con la norma EN 10088 son inertes y resistentes a la corrosión en el suelo. El potencial de corrosión libre de los aceros inoxidables altamente aleados en suelos normalmente aireados se encuentra mayormente cercano al valor del cobre. Los aceros inoxidables contendrán, como mínimo, un dieciséis por ciento de cromo, un cinco por ciento de níquel y un dos por ciento de molibdeno. Mediciones extensivas han demostrado que solo un acero inoxidable altamente aleado con el material N°. 1.4571, por ejemplo, es lo suficientemente resistente a la corrosión en el suelo.
- Otros materiales. Pueden utilizarse otros materiales si son particularmente resistentes a la corrosión en determinados entornos o resultan, por lo menos, tan buenos como los materiales listados en la tabla 3.
El proyecto de investigación titulado “Comportamiento de la corrosión de los materiales de los electrodos de puesta a tierra" ha descubierto lo siguiente respecto de la elección de los materiales de los electrodos de puesta a tierra, particularmente en lo que respeta a la combinación de diferentes materiales: se espera un mayor grado de corrosión si la relación de las superficies es AC/AA > 100.
Por lo general, se puede suponer que el material con el potencial más positivo será el cátodo. El ánodo de una celda de corrosión realmente presente puede ser reconocido por el hecho de que posee el potencial más negativo al abrir la conexión conductora del metal.
Para la conexión de instalaciones de acero en el suelo, los siguientes materiales de electrodos de puesta a tierra se comportan siempre como cátodos en los suelos (de cobertura):
- Cobre desnudo
- Cobre revestido en latón
- Acero inoxidable altamente aleado
En sobretensiones inminentes, la vía de chispa de separación opera e interconecta las instalaciones durante el tiempo que duran las sobretensiones. Sin embargo, este tipo de vías no debe instalarse para electrodos de puesta a tierra operativos y de protección, pues estos siempre deben estar conectados a la planta.
Si los cables de conexión corren subterráneamente, el acero galvanizado debe estar embebido en hormigón o en vainas sintéticas o, alternativamente, se deberán utilizar orejetas de conexión con terminales de conexión a tierra de cable NYY, o terminales de acero inoxidable de toma de tierra.
Dentro de la mampostería, los conductores de tierra pueden ser llevados hacia arriba, sin protección anticorrosiva.
Por lo general, los recubrimientos de brea no bastan. Las vainas que no absorben humedad ofrecen protección, por ejemplo, las fajas de caucho de butilo o fundas termocontraíbles.
Traducción al español del punto 5.5.7 Corrosion of earth electrodes. DEHN + SÖHNE. Lightning Protection Guide, 2 edition; September. 2007.